Hexafluoreto de enxofre
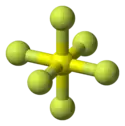
O hexafluoreto de enxofre é um composto químico inorgânico formado pelos elementos químicos enxofre e flúor, com a fórmula química SF6. O gás hexafloureto de enxofre é formado por sete átomos, em que um é central. A geometria dessa molécula denomina-se octaédrica.
| Hexafluoreto de enxofre Alerta sobre risco à saúde | |
|---|---|
 | |
 | |
 | |
| Nome IUPAC | fluoreto de enxofre (VI) |
| Outros nomes | hexafluoreto de enxofre |
| Identificadores | |
| Número CAS | |
| Número RTECS | WS4900000 |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | SF6 |
| Riscos associados | |
| MSDS | External MSDS |
| Principais riscos associados |
Gás inerte, asfixiante simples em concentrações altas. |
| Compostos relacionados | |
| Compostos relacionados | tetrafluoreto de enxofre (SF4), tetrafluoreto de carbono (CF4) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Essa molécula apresenta-se como um gás sintético, utilizado principalmente pela indústria elétrica, como meio isolante e extintor de arco eléctrico, tanto em disjuntores, como em uma subestação blindada.
É formado por um átomo de enxofre rodeado por 6 átomos de flúor. Possui grande electronegatividade, razão pela qual extingue arcos eléctricos. É quimicamente inerte, mas é 23.900 vezes mais nocivo para o efeito estufa que o dióxido de carbono. Entretanto, representa menos de 1% da colaboração no aquecimento global.
Uma curiosidade sobre esse gás é que, ao ser inalado, ele torna a voz mais grave, efeito contrário ao do gás hélio. Isso ocorre porque é um gás 5 vezes mais denso que o ar, o que aumenta o comprimento de onda das ondas sonoras. Apesar de não ser um gás tóxico, por ser mais denso que o ar, expulsa o oxigénio em ambientes fechados e de pouco espaço, causando asfixia.
Além disso, é frequentemente usado na experiência da água invisível, na qual se enche um aquário com hexafluoreto de enxofre e se coloca um 'barco' feito de alumínio. Como esse está cheio de ar, flutua como se estivesse sobre a água.
Também foi o gás utilizado nas sapatilhas Nike Air, antes de ser substituído por nitrogénio.