Brometo de magnésio
Brometo de magnésio (MgBr2) é um composto químico de magnésio e bromo que é branco e deliquescente. É frequentemente utilizado como um sedativo leve e como um anticonvulsivo para o tratamento de perturbações do sistema nervoso.[4] É solúvel em água e pouco solúvel em álcool. Pode ser encontrado naturalmente em pequenas quantidades em alguns minerais, tais como: bischofita e carnalita, e na água do mar, tal como a do Mar Morto.[5][6]
| Brometo de magnésio Alerta sobre risco à saúde[1] | |
|---|---|
 | |
 | |
| Identificadores | |
| Número CAS | ,(anidro) [13446-53-2] (hexaidrato) [75198-45-7] (decaidrato) |
| PubChem | |
| ChemSpider | |
| SMILES |
|
| InChI | 1/2BrH.Mg/h2*1H;/q;;+2/p-2 |
| Propriedades | |
| Fórmula molecular | MgBr2 (anidro) MgBr2·6H2O (hexaidrato) |
| Massa molar | 184.113 g/mol (anidro) 292.204 g/mol (hexaidrato) |
| Aparência | cristais hexagonais brancos higroscópicos (anidro), cristais monoclínicos (hexaidrato) |
| Densidade | 3,72 g·cm-3 (25 °C)[2] |
| Ponto de fusão |
711 °C[2] |
| Solubilidade em água | solúvel (1015 g·l-1 a 20 °C)[3] |
| Solubilidade | etanol: 6.9 g/100 mL (20 °C) |
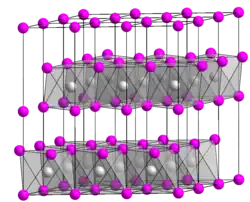
| Estrutura | |
| Estrutura cristalina | romboédrico, hP3, Grupo espacial = P-3m1, No. 164 |
| Geometria de coordenação |
octaédrico |
| Termoquímica | |
| Entalpia padrão de formação ΔfH |
-524.3 kJ·mol-1 |
| Entropia molar padrão S |
117.2 J·mol-1·K-1 |
| Riscos associados | |
| Índice UE | Não listado |
| Frases R | R36/37/38 |
| Frases S | S26 S36 |
| Compostos relacionados | |
| Outros aniões/ânions | fluoreto de magnésio cloreto de magnésio iodeto de magnésio |
| Outros catiões/cátions | brometo de berílio brometo de cálcio brometo de estrôncio brometo de bário brometo de rádio |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Síntese
Brometo de magnésio pode ser sintetizado por reacção de ácido bromídrico com óxido de magnésio e cristalizando-se o produto.[6] Também pode ser produzido pela reação de carbonato de magnésio e ácido bromídrico, e recolhendo-se o sólido resultante após evaporação.[5]
Uma via alternativa é a adição de magnésio a uma solução de amônia líquida e brometo de sódio, em seguida, evaporando o solvente e recolhendo-se o precipitado.[7]
Usos
Brometo de magnésio é utilizado como um catalisador para muitas reacções, tipicamente como um solvente ou utilizado como um reagente de Grignard.[carece de fontes]
Referências
- Lide, David R. (1998). Handbook of Chemistry and Physics 87 ed. Boca Raton, FL: CRC Press. pp. 4–67. ISBN 0-8493-0594-2
- Catálogo da Sigma-Aldrich, Brometo de magnésio, consultado em 9 de abril de 2011
- Sicherheitsdatenblatt Strem
- Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- Gruyter, W. Conise Encyclopedia Chemistry, Walter de Gruyter & Company: Berlin, 1993; 612
- Lewis, R.J. Hawley’s Condensed Chemical Dictionary, 15th ed.; John Wiley &Sons Inc.:New York, 2007; 777
- Jacobson, C.A. Encyclopedia of Chemical Reactions, Reinhold Publishing Corporation: New York, 1951; 409