Malonato de dietila
Malonato de dietila, também conhecido como DEM, é o éster dietílico do ácido malônico. Ocorre naturalmente em uvas e morangos como líquido incolor com odor de maçã, e é usado em perfumes. É também usado na síntese de outros compostos tais como barbituratos, aromatizantes artificiais, vitamina B1 e vitamina B6.
| Malonato de dietila Alerta sobre risco à saúde | |
|---|---|
 | |
 | |
| Nome IUPAC | Propaodiato de 1,3-dietila |
| Identificadores | |
| Abreviação | DEM |
| Número CAS | |
| PubChem | |
| Número EINECS | |
| ChemSpider | |
| MeSH | |
| ChEBI | |
| Número RTECS | OO0700000 |
| SMILES |
|
| InChI | 1/C7H12O4/c1-3-10-6(8)5-7(9)11-4-2/h3-5H2,1-2H3 |
| Referência Beilstein | 774687 |
| Propriedades | |
| Fórmula molecular | C7H12O4 |
| Massa molar | 160.17 g/mol |
| Aparência | líquido incolor |
| Densidade | 1.05 g/cm3, líquido |
| Ponto de fusão |
−50 °C (223 K) |
| Ponto de ebulição |
199 °C (472 K) |
| Solubilidade em água | desprezível |
| Riscos associados | |
| MSDS | Oxford University MSDS |
| Principais riscos associados |
Perigoso (X), Inflamável (F) |
| Ponto de fulgor | 200 °C |
| Compostos relacionados | |
| Ésteres relacionados | Malonato de dimetila Oxalato de dietila Pirocarbonato de dietila |
| Compostos relacionados | Ácido malônico |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Estrutura e propriedades
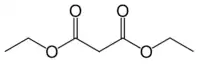
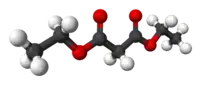
Ácido malônico é um ácido dicarboxílico bem simples, com dois grupos carboxila bem próximos na molécula. Na formação do malonato de dietila a partir do ácido malônico, o grupo hidroxila (-OH) de ambos os grupos carboxila é substituído por um grupo etóxi (-OEt; -OCH2CH3). O grupo metileno (-CH2-) no meio da parte malônica da molécula do DEM é vizinho de dois grupos carbonila (-C(=O)-).[1]
Preparação
Malonato de dietila pode ser preparado reagindo o sal de sódio do ácido cloroacético com cianeto de sódio, seguido de hidrólise básica do nitrilo formado para dar o sal de sódio do ácido malônico. Obtém-se o malonato de dietila por meio da esterificação de Fischer:
Reações
Outras reações
Como muitos outros ésteres, este composto sofre condensação de ésteres de Claisen. A vantagem do uso deste composto é que reações de autocondensação indesejáveis são evitadas. Também sofre bromação na posição alfa.[2]
Referências
- «IR spectrum of Malonic acid». Consultado em 29 de junho de 2011. Arquivado do original em 26 de junho de 2010
- C. S. Palmer and P. W. McWherter. «Ethyl Bromoacetate». Org. Synth.; Coll. Vol., 1