Ácido tríflico
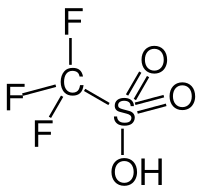
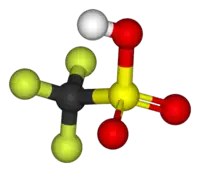
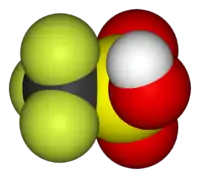
O ácido trifluormetanossulfônico ou ácido tríflico é um ácido sulfônico de fórmula molecular CF3SO3H, também representado por TfOH. É um dos mais fortes ácidos conhecidos, sendo classificado como superácido por ser em torno de mil vezes mais forte que o ácido sulfúrico.[1]
| Ácido tríflico Alerta sobre risco à saúde | |
|---|---|
 | |
 | |
 | |
| Nome IUPAC | Ácido trifluormetanossulfônico |
| Outros nomes | Ácido tríflico |
| Identificadores | |
| Número CAS | |
| Propriedades | |
| Fórmula molecular | CF3SO3H |
| Massa molar | 150.08 g/mol |
| Aparência | Líquido incolor |
| Densidade | 1.696 g/mL |
| Ponto de fusão |
-40 °C |
| Ponto de ebulição |
162 °C |
| Solubilidade em água | Miscível |
| Riscos associados | |
| Principais riscos associados |
Corrosivo, irritante aos olhos. |
| Compostos relacionados | |
| Outros catiões/cátions | Triflato de lítio |
| Compostos relacionados | Ácido difluormetanossulfônico Ácido triclorometanossulfônico Ácido trifluoroacético |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Produção
Uma das várias rotas de síntese deste composto é a oxidação do derivado fluorado do metanotiol com peróxido de hidrogênio.
Segurança
O ácido tríflico em contato com a pele causa queimaduras graves e destruição dos tecidos. Na inalação, causa espasmos fatais, inflamação e edema.
Usos
É usado como catalisador em várias reações da química orgânica, já que sua base conjugada é um ótimo grupo de saída. Ao contrário do ácido sulfúrico, não "sulfona" aromáticos.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.